问题
计算题
水垢的主要成分是CaCO3和Mg(OH)2,为了测定其中CaCO3的含量,取100g水垢,加入过量稀盐酸,测量5min内生成的CO2的质量,绘出如下图所示曲线,请问:
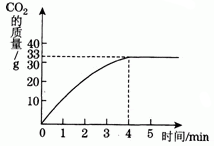
(1)该水垢中CaCO3的质量分数为多少?
(2)假定水垢不含其他杂质,若要计算反应消耗的稀盐酸的质量,还需知道什么信息?
答案
解:(1)由图可知共生成33gCO2
设1009水垢中含碳酸钙的质量为x
CaCO3+2HCl==CaCl2+CO2↑+H2O
100 44
x 33g
x=75g
75g/100g×100%= 75%
(2)还要知道稀盐酸的质量分数
