问题
计算题
称取铜、锌混合物粉末10.0g置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49.0g稀硫酸,剩余固体3.5g。
(1)该混合物粉末中铜的质量分数为多少?
(2)所用的稀硫酸溶质的质量分数是多少?
答案
(1)铜的质量分数=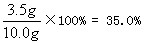
(2)设所用稀硫酸溶质的质量分数为x
Zn+H2SO4==ZnSO4+H2↑
65 98
10.0g-3.5g 49g×x
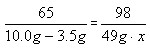
x= 20.0%
称取铜、锌混合物粉末10.0g置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49.0g稀硫酸,剩余固体3.5g。
(1)该混合物粉末中铜的质量分数为多少?
(2)所用的稀硫酸溶质的质量分数是多少?
(1)铜的质量分数=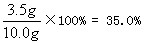
(2)设所用稀硫酸溶质的质量分数为x
Zn+H2SO4==ZnSO4+H2↑
65 98
10.0g-3.5g 49g×x
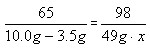
x= 20.0%