问题
计算题
工业上用电解NaCl溶液的方法来制取NaOH、Cl2和H2,反应的化学方程式为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液214.6g进行电解,当NaCl完全反应时,生成0.4gH2。
2NaOH+H2↑+Cl2↑。现取一定质量分数的NaCl溶液214.6g进行电解,当NaCl完全反应时,生成0.4gH2。
(1)当NaCl完全反应时,生成Cl2的质量为________g,参加反应的NaCl的质量为________g。
(2)当NaCl完全反应时,所得NaOH溶液中溶质的质量分数为多少?(假设生成的Cl2和H2全部逸出)
答案
(1)14.2克;23.4克
(2)解:设生成NaOH的质量为x。
2NaCl+2H2O==2NaOH+H2↑+Cl2↑
80 2
x 0.4g
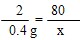
解得: x=16g
则NaOH的质量分数=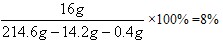
答:所得NaOH溶液中溶质的质量分数为8%。
