问题
计算题
一定质量10%的A溶液和一定质量10%的CaCl2溶液恰好完全反应,生成白色沉淀B,化学方程式为:
A+CaCl2=B↓+2NaCl(已配平)。
(1)A物质必定含有的金属元素是_______,A和B的相对分子质量之差为______。
(2)滤出沉淀B,加入足量稀盐酸,B逐渐溶解,收集到无色无味的气体4.4g。求滤出B后所得溶液中NaCl的质量分数。
答案
(1)Na;6
(2)解:设CaCO3的质量为x ;
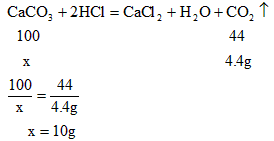
设Na2CO3溶液的质量为y,CaCl2溶液的质量为z,NaCl的质量为a
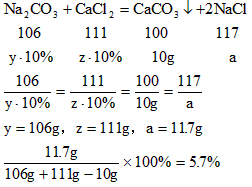
答:滤出B后所得溶液中NaCl的质量分数为5.7%。
