问题
计算题
用15.5mL 稀盐酸恰好能溶解4.24g 带铁锈(Fe2O3) 的铁片,生成的气体在标准状况下的体积为0.616L ,向反应后的溶液中滴入少量的KSCN 溶液不显红色。
(1) 求盐酸的物质的量浓度。
(2) 铁片里铁单质的质量分数。
答案
解:设4.24g 样品中Fe 的物质的量为xmol ,Fe2O3为ymol 。
已知 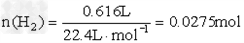
Fe + 2HCl == FeCl2 + H2↑
0.0275mol 0.0275mol 0.0275mol
由关系式: Fe2O3 -- 2FeCl3 -- Fe -- 3Fe2+
ymol (x-0.0275)mol 3ymol
依题意有 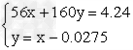
x=0.04 y=0.0125
n(HCl)=2n(Fe2+)=(0.04mol+2×0.0125mol)×2=0.13mol
(1)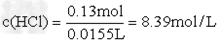
(2)