问题
计算题
“黄铜”是铜锌合金,具有较强机械性能,街头许多“金色”饰品就是用它来制作的.某研究性学习小组为了测定黄铜中铜的质量分数,称取20g黄铜样品,放入烧杯中,然后加入某浓度的稀盐酸100 g(足量),用玻璃棒搅拌至不再产生气泡为止(反应的化学方程式为:Zn+2HCl==ZnCl2+H2↑),称量剩余物质的总质量为119.8g.请计算:
(1)实验过程中,产生氢气的质量 _________ ,你的计算依据是 _________ .
(2)该铜锌合金中铜的质量分数.
答案
(1)0.2g;质量守恒定律;
(2)设反应消耗锌的质量为x;
Zn+2HCl==ZnCl2+H2↑
65 2
x 0.2g
65:2=x:0.2g
解之得:x=6.5g;
该铜锌合金中铜的质量为:20g﹣6.5g=13.5g,
则该铜锌合金中铜的质量分数为: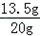 ×100%=67.5%.
×100%=67.5%.
答:该铜锌合金中铜的质量分数为67.5%.
