下图是“×××钙片商品标签图”(最后结果保留在小数点后一位)
×××儿童咀嚼片 |
| (60片装) |
| [主要成分]碳酸钙,维生素D |
| [规格]2.5g/片,每片中含碳酸钙≥1.24g,维生素D 100 l.U. |
| [食用方法]嚼食,每天一片 |
| [功效]补钙 |
根据标签内容信息,计算回答下列问题:
③通过计算判断钙片中碳酸钙的含量标注是否属实。
(1)40%; 0.5
(2)解:①根据质量守恒定律可知。生成二氧化碳的质量为: 40g + 4×2.5g -47.8g = 2.2g
② 设参加反应的CaCO3和HCl的质量分别为x和y
CaCO3 + 2HCl ==CaCl2 + H2O + CO2 ↑
100 73 44
x y 2.2g
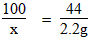
x=5g
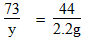
y=3.65g
则稀盐酸中溶质的质量分数为: 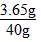 ×100% =9.1%
×100% =9.1%
③每片中含CaCO3的质量为: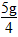 =1.25g>1.24g,故钙片中碳酸钙的含量标注属实。
=1.25g>1.24g,故钙片中碳酸钙的含量标注属实。
答:①生成二氧化碳的质量为2.2g;
②稀盐酸中溶质的质量分数为9.1%;
③通过计算判断钙片中碳酸钙的含量标注属实。
