问题
问答题
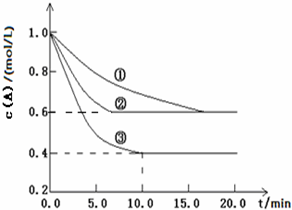
在溶液中,反应A+2B⇌C分别在三种不同实验条件下进行,它们的起始浓度均为 c(A)=1.0mol/L,c(B)=2.0mol/L及c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件是:②______;③______;
(2)实验②平衡时B的转化率为______;
(3)该反应的△H______0(填>”或<”)(4)该反应进行到10min时的平均反应速率:______(以③计算).
答案
(1)与①比较,②反应速率增大,但与①处于同一平衡状态,则②应为加入催化剂,与①比较,③反应速率增大,可能是升高温度或增大压强,但如是增大压强,减小容器的体积虽然平衡向正反应方向移动,但A的平衡浓度反而增大,不符合图象,则应为升高温度,
故答案为:加催化剂;升高温度;
(2)实验②平衡时B的转化率为
×100%=40%,1.0mol/L-0.6mol/L 1.0mol/L
故答案为:40%;
(3)由图象③可以看出,升高温度,A的浓度降低,说明升高温度平衡向正反应方向移动,则正反应为吸热反应,
故答案为:>;
(4)该反应进行到10min时的平均反应速率为:v=
=△c △t
=0.06mol/(L•min),1.0mol/L-0.4mol/L 10min
故答案为:0.06 mol/(L•min).
