工业炼铁是把铁矿石和焦炭等原料一起加入高炉,在高温下通入空气进行一系列反应把铁还原出来.
(1)赤铁矿(主要成分为Fe2O3)在高炉里反应生成单质铁的化学方程式是 _________ .
(2)计算:
①5000t含氧化铁84%的赤铁矿中,氧化铁的质量是?
②上述赤铁矿理论上可炼得含铁98%的生铁的质量是?
解:(1)Fe2O3+3CO 3CO2+2Fe;
3CO2+2Fe;
(2)①由5000t含氧化铁84%的赤铁矿,则氧化铁的质量为5000t×84%=4200t,
②设可炼得含铁98%的生铁xt,则
Fe2O3+3CO 3CO2+2Fe
3CO2+2Fe
160 112
4200t x×98%
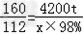
解得x=3000t,即可炼得含铁98%的生铁3000t。

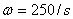 。将发电机的输出端接入图中的装置K后,装置K能使交流电变成直流电,而不改变其电压的大小。直流电的另一个输出端与一可变电阻R相连,可变电阻的另一端P是直流电的正极,直流电的另一个输出端Q是它的负极。
。将发电机的输出端接入图中的装置K后,装置K能使交流电变成直流电,而不改变其电压的大小。直流电的另一个输出端与一可变电阻R相连,可变电阻的另一端P是直流电的正极,直流电的另一个输出端Q是它的负极。