问题
计算题
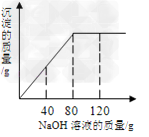
某同学在实验室发现一瓶标签残缺的氯化镁溶液.为了测定此溶液的溶质质量分数,他取出一定量的该溶液,向其中逐滴加入溶质质量分数为5%的氢氧化钠溶液.反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如下图所示.
【反应的化学方程式为MgCl2+2NaOH==2NaCl+Mg(OH)2↓】
(1)当氢氧化钠溶液为_________g时,氯化镁与氢氧化钠恰好完全反应,这时沉淀的质量为_________g.
(2)若反应中所用氯化镁溶液的质量为100g,请计算该氯化镁溶液的溶质质量分数?
答案
(1)80;2.9
根据反应的曲线,可知当加入80g氢氧化钠溶液时恰好完全反应;此时反应消耗氢氧化钠的质量=80g×5%=4g.
设生成沉淀的质量为x,参加反应的氯化镁的质量为y
MgCl2+2NaOH==Mg(OH)2↓+2NaCl
95 80 58
y 4g x

x=2.9g,y=4.75g
(2)该氯化镁溶液的溶质质量分数= ×100%=
×100%=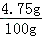 ×100%=4.75%
×100%=4.75%
