问题
计算题
某化学活动小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品,投入装有50.0g稀盐酸(足量)的烧杯中(烧杯质量也为50.0g,样品中杂质不与酸反应).在实验过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
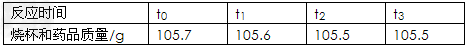
(1)反应中产生氢气 _________ g;
(2)这种钢样品中铁的质量分数是多少?(精确到0.1%)
(3)有同学提出:在氧气中灼烧钢样品可使碳变为二氧化碳跑掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了许多.原因是_________.
答案
(1)0.2;
(2)设样品中含铁的质量为x.
Fe+2HCl=FeCl2+H2↑
56 2
x 0.2g

x=5.6g
钢样品中铁的质量分数=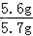 ×100%=98.2%
×100%=98.2%
答:这种钢样品中铁的质量分数是98.2%;
(3)因为碳减少的质量,远小于铁转化为氧化物增加的质量.
