问题
计算题
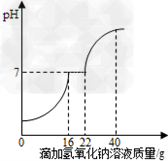
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是应为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如下图所示的关系.求该工业盐酸中氯化铁的溶质质量分数.(结果保留至0.1%)
答案
解:根据图中信息可知:与氯化铁反应的氢氧化钠溶液的质量为22g﹣16g=6g;
设20g该工业盐酸中氯化铁的质量为x
FeCl3+3NaOH=Fe(OH)3↓+3NaCl
162.5 120
x 6g×10%=0.6g
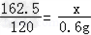
解得:x=0.8125g
该工业盐酸中氯化铁的质量分数为
 ×100%=4.1%
×100%=4.1%
答:该工业盐酸中氯化铁的质量分数为4.1%.
