问题
计算题
某碳酸钠样品中含有少量氯化钠杂质。现将一定量样品放入烧杯中,称得总质量为163. 9g,加入146.1g氯化钙溶液,恰好完全反应,产生沉淀10g,过滤后,所得溶液中溶质的质量分数为10%,计算样品中Na2CO3的质量分数? (反应方程式为:Na2CO3 +CaCl2 === 2NaCl + CaCO3↓)
答案
解:设样品中NaCl的质量为m,样品中Na2CO3的质量为x,生成的NaCl的质量为y
Na2CO3 + CaCl2 = 2NaCl + CaCO3↓
106 117 100
x y 10g

10.6g + m + 146.1g - 10g = (11.7g +m) ÷10% , m= 3.3g
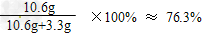
答:样品中Na2CO3的质量分数为76.3%。
