在一烧杯中盛有42.2g碳酸钙和氯化钙的粉末状混 合物,向其中加入116.6g水,使氯化钙完全溶解。然后向其 中逐滴加入10%的稀盐酸,烧杯中剩余固体的质量与加入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:
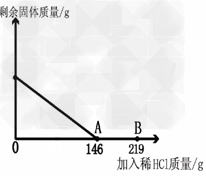
(1)当滴入稀盐酸质量至图中A点时,求所得溶液中溶质的质量分数。
(2)当滴入稀盐酸质量至图中B点时,继续向烧杯中加入上述粉末状混合物至刚刚无气泡产生,求此时烧杯中钙元素质量。
(1) 146 g×10%=14.6 g
设13.5g样品中碳酸钙的质量为x, 生成氯化钙的质量为y,产生二氧化碳质量为z
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 73 111 44
x 14.6g y z
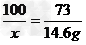 x=20g
x=20g
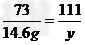 y=22.2 g
y=22.2 g
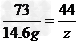 z=8.8 g
z=8.8 g
44.2g-20g=22.2g
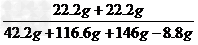 ×100%=15%
×100%=15%
(2)22.2g+22.2 g+22.2g=66.6g
66.6g ×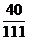 ×100%=24g
×100%=24g
答:溶液中溶质的质量分数为15%,
烧杯中钙元素的质量为24g。