碘是重要的无机化工原料,海藻灰化法是我国目前制碘的主要方法。某研究性学习小组查阅文献,设计并进行了以下模拟实验。
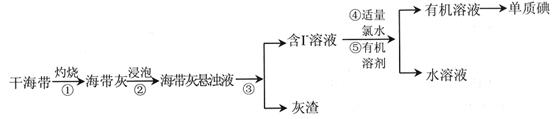
请回答:
(1)步骤①中灼烧海带用到的实验仪器是______________________(填序号)。
a. 试管 b. 坩埚 c. 烧杯
(2)步骤③的实验操作是_______________________。
(3)步骤④中反应的离子方程式是_____________________________________。
(4)步骤⑤中,可以选择的有机溶剂是__________________(填序号)。
a. 乙酸 b. 四氯化碳 c. 酒精 d. 苯
(5)同学们观察到完成步骤⑤后,所得到的水溶液呈淡黄色。某同学推断其中可能含有碘单质,检验方法是: __________________________________________________________________________。
(6)因过量的Cl2会与I2反应,所以步骤④中加入的氯水应保持适量。为证明此说法,某同学做如下实验:取少量碘水,滴加氯水,观察到碘水逐渐褪色,经检验生成物含有IO3-。该反应的化学方程式是_________________________________。
(9分)(1)b(1分)(2)过滤(1分) (3)Cl2+2I-=2Cl-+I2(2分)
(4)bd(1分,错选为0分,少选为0.5分)
(5)取少量溶液于试管中,滴入几滴淀粉溶液,若溶液呈蓝色,证明溶液中还含有I2。
(2分,取样、试剂、现象、结论各0.5分,若试剂错为0分)
(6)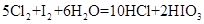 (2分)
(2分)
题目分析:(1)固体灼烧需要在坩埚中进行,所以步骤①中灼烧海带用到的实验仪器是坩埚,答案选b。
(2)步骤③的的目的是分离出灰渣和含有碘离子碘溶液,所以实验操作是过滤。
(3)氯水具有强氧化性,能把碘离子氧化生成单质碘,反应的离子方程式是Cl2+2I-=2Cl-+I2。
(4)步骤⑤是萃取,萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,选用的萃取剂的原则是:①和原溶液中的溶剂互不相溶更不能发生化学反应;②溶质在该溶剂中溶解度要远大于原溶剂。乙酸和乙醇都是与水互溶的,所以可以选择的有机溶剂是苯和四氯化碳,答案选bd。
(5)因为单质碘能和淀粉发生显色反应,而使显蓝色,据此可以鉴别。即取少量溶液于试管中,滴入几滴淀粉溶液,若溶液呈蓝色,证明溶液中还含有I2。
(6)经检验生成物含有IO3-,即单质碘被氧化生成了IO3-,而还原产物是氯化氢,所以反应的离子方程式是5Cl2+I2+6H2O=2HIO3+10HCl。
点评:该题是高考中的常见题型,属于中等难度的试题。试题易碘的提取为载体,涉及仪器的选择、物质的分离和提纯、方程式的书写、萃取剂的选择以及单质碘的检验,有利于激发学生的学习兴趣,增强学生的学习积极性。
