问题
计算题
取铜和氧化铜的混合物10g,加入一定量的稀硫酸,测得恰好完全反应后,得到溶质质量分数为16%的溶液100g.计算
(1)固体混合物中铜的质量分数.
(2)稀硫酸的溶质质量分数.
答案
解:反应后所得溶液中的溶质为硫酸铜,质量为16%×100g=16g
设参加反应的氧化铜的质量为x,参加反应的硫酸质量为y
CuO+H2SO4═CuSO4+H2O
80 98 160
x y 16g
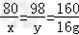 解之得:x=8g,y=9.8g
解之得:x=8g,y=9.8g
所以原混合物中铜的质量为10g﹣8g=2g
(1)原混合物中铜的质量分数=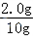 ×100%=20%,
×100%=20%,
(2)加入的稀硫酸的质量为所得溶液的质量减去氧化铜的质量,即100g﹣8g=92g所以稀硫酸的溶质质量分数=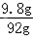 ×100%=10.7%
×100%=10.7%
答:(1)原混合物中铜的质量分数20%,(2)稀硫酸的溶质质量分数10.7%.
