问题
计算题
某化学兴趣小组的同学采集了一些大理石样品,为测定该样品中碳酸钙的质量分数,取样品6g粉碎成粉末状置于烧杯中,向其中加入10%的稀盐酸并不断搅拌,恰好不再有气泡产生时(已知杂质不与稀盐酸反应),共用去稀盐酸36.5g。
(1)该实验中能否用稀硫酸代替稀盐酸____(填“能”或“不能”)。
(2)用质量分数为36%的浓盐酸100g能配制所需10%的稀盐酸____g。
(3)计算样品中碳酸钙的质量分数。(结果保留到0.1%)
答案
解:(1)能
(2)360
(3)设6g样品中CaCO3的质量为x
CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
100 73
x 36.5g×10%
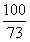 =
=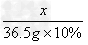
x=5g
样品中碳酸钙的质量分数为: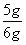 ×100%=83.3%
×100%=83.3%
答:样品中碳酸钙的质量分数为83.3%。
