某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:

(1)下列实验方案适用于在实验室制取所需SO2的是 ;
A.Na2SO3溶液与HNO3
B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧
D.碳与热浓H2SO4
(2)写出SO2气体通入A中的离子反应___________________________________________;
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,
取A中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加 入新制的氯水,溶液变红
入新制的氯水,溶液变红
上述方案不合理的是 ,原因是 ;
(4)能表明I-的还原性弱于SO2的现象是 。
(5)下图为SO2的制备和收集装置图:(夹持仪器省略)

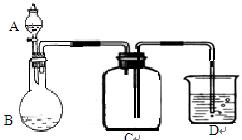
仪器A名称 ,图中的装置错误的是 (填“A、B、C、D”的一个或多个)
该装置气密性检查的操作是
。
(1)B (1分)
(2)2Fe3+ + SO2 + 2H2O= SO42 +2Fe3+ + 4 H+(2分)
(3)①(2分);SO2过量,SO2可使KMnO4溶液褪色 (2分)
(4)B中蓝色褪去(2分)
(5)分液漏斗(1分) 收集装置C中导气管短进长出错误(2分) 关闭分液漏斗活塞,向D烧杯中加水至浸没导气管下端管口,用热毛巾加热圆底烧瓶,导管口有气泡,停止加热后,导管内形成一段水柱,则该装置气密性良好。(4分)
