问题
计算题
研究性学习:探究实验室中久置的NaOH的变质程度
[研究方案]先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量.从而进一步确定样品中NaOH的变质程度.
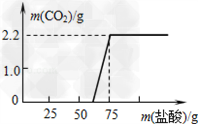
(1)实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.填写下表:(计算结果保留小数点后一位)
| Na2CO3的质量/g | |
| 变质NaOH的质量/g | |
| NOH的变质程度 (用质量分数表示) | |
(2)求实验过程中与NaOH反应所用盐酸的质量.
答案
(1)
(2)没变质氢氧化钠质量为13.3g﹣5.3g=8g
设参加反应氯化氢的质量为m
NaOH+HCl=NaCl+H2O
40 36.58g
8g m
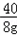 =
=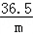 m=8g×
m=8g×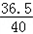 =7.3g;
=7.3g;
盐酸的质量= ×100%=50g.
×100%=50g.
(3)NaOH被中和后,滴加盐酸,为什么没有立即产生CO2气体.
