问题
计算题
取已部分风化的碳酸钠晶体10.7克,溶于水制成饱和溶液,逐滴加入足量的饱和澄清石灰水使其完全反应,然后过滤.将所得的固体经洗涤、烘干后高温灼烧至重量不再减少为止,得白色固体2.8克.计算这种碳酸钠晶体的结晶水失去的百分率是多少?
答案
解:物质间转化的化学反应是:
Na2CO3·10H2O==Na2CO3+10H2O
Na2CO3+Ca(OH)2==CaCO3↓+2NaOH
CaCO3 CaO+CO2↑
CaO+CO2↑
烘干后高温灼烧至重量不再减少为止,得白色固体2.8,
根据以上化学反应可知该白色固体是氧化钙.设未风化的碳酸钠晶体的质量是X,其中碳酸钠的质量是Y
由以上反应可知物质间的关系是:
Na2CO3·10H2O~Na2CO3~CaCO3~CaO
286 106 56
X Y 2.8g
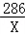 =
=
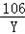 =
=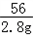
X=14.3g Y=5.3g
所以碳酸钠晶体失去的结晶水的质量是:14.3g﹣10.7g=3.6g,
碳酸钠晶体中结晶水的质量是:14.3g﹣5.3g=9g
所以碳酸钠晶体的结晶水失去的百分率=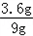 ×100%=40%
×100%=40%
答:碳酸钠晶体的结晶水失去的百分率是40%.
