实验室以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)为原料制取CaCl2·H2O和CaO2的主要流程如下:
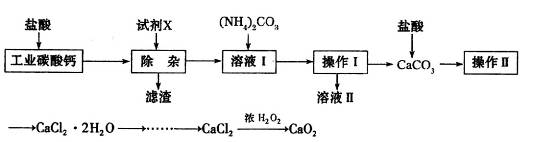
(1)加入试剂X,调节溶液pH为碱性环境,以除去溶液中Al3+和Fe3+,滤渣的主要成分是___________。试剂X可以选择下列的________(填编号)。
A.CaO
B.CaCO3
C.NH3·H2O
D.Ba(OH)2(2)操作II中进行蒸发浓缩时,除三角架、酒精灯外,还需要的仪器有__________。
(3)由CaCl2制取CaO2的反应中,温度不宜太高的原因是_______________。
(4)用下列装置测定工业碳酸钙的质量分数
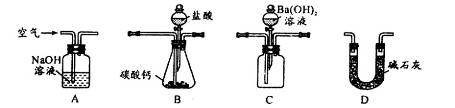
①检验装置B气密性良好的实验过程是__________________________。
②按A—B—C—D顺序连接,然后从A装置通入空气,目的是_______________。
③装置D的作用为______________________。
④实验时,准确称取10.00g工业碳酸钙3份,进行3次测定,测得BaCO3沉淀的平均质量为17.73g,则样品中CaCO3的质量分数为__________________。
(除去注明外,每空2分,共14分)(1)Fe(OH)3和Al(OH)3 AC (2)蒸发皿、玻璃棒(坩埚钳)
(3)防止温度过高H2O2分解
(4)①关闭分液漏斗的活塞,用止水夹夹住左边(或右边或不用)橡皮管处,将右边(或左边或两边)导气管插入水中,微热B装置,发现导气管有气泡产生,冷却后,导气管有一段液柱形成,注明气密性良好(合理即可) ②排净装置中二氧化碳(1分)
③防止空气中CO2与Ba(OH)2溶液反应(1分) ④90%
题目分析:(1)在碱性条件下,Al3+、Fe3+分别生成氢氧化铝和氢氧化铁沉淀,所以滤渣的主要成分是Fe(OH)3和Al(OH)3;由于实验室以工业碳酸钙为原料制取CaCl2·H2O和CaO2的,所以试剂X不能选用碳酸钙。又因为不能引入新的杂质,所以不能选择氢氧化钡,可以选择氧化钙。由于后续实验中加入碳酸铵,所以X还可以是氨水,即答案选AC。
(2)由于氯化钙易溶于水,所以要得到氯化钙晶体,应该是蒸发浓缩冷却结晶,所以操作II中进行蒸发浓缩时,除三角架、酒精灯外,还需要的仪器有蒸发皿、玻璃棒(坩埚钳)。
(3)由CaCl2制取CaO2的反应中,需要双氧水参加。由于双氧水易分解,所以温度不宜太高的原因是)防止温度过高H2O2分解。
(4)①由于B装置中含有分液漏斗,所以要检验其气密性,正确的操作应该是关闭分液漏斗的活塞,用止水夹夹住左边(或右边或不用)橡皮管处,将右边(或左边或两边)导气管插入水中,微热B装置,发现导气管有气泡产生,冷却后,导气管有一段液柱形成,注明气密性良好。
②实验原理是利用盐酸和碳酸钙反应生成CO2,CO2被氢氧化钡吸收生成碳酸钡沉淀,然后通过称量C装置的即可。由于在反应中装置中会残留CO2,所以通入空气的目的是排净装置中二氧化碳。
③由于空气中含有CO2,因此D装置中碱石灰的作用是防止空气中CO2与Ba(OH)2溶液反应。
④根据碳原子守恒可知,CaCO3的质量是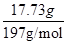 ×100g/mol=9.00g,所以样品中CaCO3的质量分数为
×100g/mol=9.00g,所以样品中CaCO3的质量分数为 ×100%=90%。
×100%=90%。
