问题
计算题
为防止有人利用假化肥坑害农民,可采用铵盐与氢氧化钠的反应来检验某些氨肥的质量。某同学称取8.25g化肥硫酸铵(杂质不含氮元素)与足量的氮氧化钠混合后,放在试管中加热,发生如下反应: ( NH4)2SO4+ 2NaOH 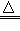 Na2SO4+ 2H2O+2NH3↑充分反应后收集到1.7g氨气,请计算:
Na2SO4+ 2H2O+2NH3↑充分反应后收集到1.7g氨气,请计算:
(1)这种化肥中硫酸铵的质量分数是多少?
(2)氮元素的质量分数是多少?
答案
(1)解:设8.25g硫酸铵化肥中含纯硫酸铵的质量为x
( NH4)2SO4+ 2NaOH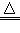 Na2SO4+ 2H2O+2NH3↑
Na2SO4+ 2H2O+2NH3↑
132 34
x 1.7g
132:34=x:1.7g x= 6.6g
该化肥中硫酸铵的质量分数为: ×100%=80%
×100%=80%
(2)该化肥中氮元素的质量分数为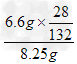 ×100%= 17%
×100%= 17%
