问题
计算题
取3份73克某浓度的盐酸,分别加入盛有NaHCO3和KHCO3
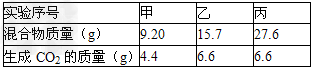
(1)盐酸的溶质质量分数为?
(2)混合物中NaHCO3和KHCO3的质量比为?
答案
解:(1)NaHCO3和KHCO3与盐酸反应的方程式分别为:
NaHCO3+HCl==NaCl+CO2↑+H2O,KHCO3+HCl==KCl+CO2↑+H2O,由方程式可知:
HCl~CO2,据此关系式进行求解;
设73克某浓度的盐酸中溶质的质量是x
HCl~CO2
36.5 44
x 6.6g
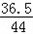 =
=
解得x=5.475g
所以所用盐酸的溶质质量分数是 ×100%=7.5%;
×100%=7.5%;
(2)用甲组数据解答;设混合物中碳酸氢钠的质量为y,则碳酸氢钾的质量为9.2g﹣y,设碳酸氢钠对应的二氧化碳的质量为z.
NaHCO3+HCl==NaCl+CO2↑+H2O
84 44
y z
 =
= ﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣①
﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣﹣①
KHCO3+HCl==KCl+CO2↑+H2O
100 44
9.2g﹣y 4.4g﹣z
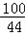 =
= ﹣﹣﹣﹣﹣﹣﹣﹣﹣②
﹣﹣﹣﹣﹣﹣﹣﹣﹣②
根据①②解得:y=4.2g,即碳酸氢钠的质量为4.2g,碳酸氢钾的质量为5g.两者质量为
4.2g:5g=21:25;
