废易拉罐的成分比较复杂,据查,铝易拉罐各部分成分及含量(质量百分含量)见表:
| Si | Fe | Cu | Mn | Mg | Cr | Zn | Ti | Al | |
| 罐身/% | 0.3 | 0.7 | 0.25 | 0.25 | 1.0~1.5 | 其余 | |||
| 罐盖/% | 0.2 | 0.35 | 0.15 | 0.2~0.5 | 4.0~5.0 | 0.1 | 0.25 | 其余 | |
| 拉环/% | 0.2 | 0.35 | 0.15 | 0.2~0.5 | 3.0~4.0 | 0.1 | 0.25 | 0.1 | 其余 |
为了验证罐身的组成成分,进行了如下实验:
【实验仪器与药品】
仪器:酒精灯、烧杯、试管、试管夹、漏斗、滤纸、铁圈、玻璃棒、砂纸、剪刀
药品:易拉罐、去污粉、NaOH溶液、KSCN溶液、盐酸、镁试剂、高碘酸(H3IO6,弱酸)
【实验方案】
实验预处理:将剪好的易拉罐片用砂纸打磨,除去表面的涂料层,直到光亮后用去污粉清洗干净备用。
【实验过程】分别向试管a、b中加入少量上述易拉罐片,进行如下操作:
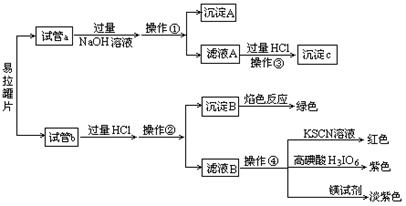
请填写下列空白:
(1)图中操作①②所用到的玻璃仪器有 。
(2)沉淀A的成分为 。
(3)操作③观察到的现象为 ;反应的离子方程式为 、
、 。
(4)若试管a、b中取样相同,则分别加入足量的NaOH溶液、稀盐酸后,相同条件下理论上产生的气体体积V(a) V(b)(填“>”、“<”或“=”)
(1)漏斗、烧杯、玻璃棒(每个1分,共3分)
(2)Fe、Cu、Mn、Mg等(全对得2分,漏写得1分,错写不得分)
(3)开始生成白色沉淀,并逐渐增多,后沉淀部分溶解(2分);H++ AlO2-+H2O=Al(OH)3↓(2分);2H++ SiO32-=H2SiO3↓(2分);Al(OH)3+3H+=Al3++3H2O(2分)(书写时不要求顺序)
(4)<(2分)
题目分析:
(1)过滤使用到的有漏斗、烧杯、玻璃棒。
(2)不溶于NaOH溶液有Fe、Cu、Mn、Mg等。
(3)Na2SiO3和NaAlO2溶液中加入盐酸开始生成白色沉淀,并逐渐增多,后沉淀部分溶解;H++ AlO2-+H2O=Al(OH)3↓;2H++ SiO32-=H2SiO3↓;Al(OH)3+3H+=Al3++3H2O。
(4)根据金属的含量可以看出与盐酸反应的金属量多,放出气体较多。
