问题
计算题
某化学兴趣小组的同学在综合实践活动中了解到,某石灰石原料,其中只含有的一种杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温下不发生分解反应).为了测定该石灰石的纯度,兴趣小组取用2g这种石灰石样品,用实验室现有的稀盐酸30g分次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表(利用实验数据绘制的图象见如图)

计算:
(1)你论为第 ____次无须实验,理由是 ________________ ;
(2)该石灰石样品的纯度是?
(3)求稀盐酸的溶质的质量分数是多少?
(4)如果该石灰石厂煅烧50t这种石灰石,最多可得到含杂质的生石灰多少吨?

答案
(1)5;第4次中盐酸已经有剩余,碳酸钙已经完全反应
(2)碳酸钙的质量=2g﹣0.3g=1.7g,石灰石样品的纯度=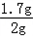 ×100%=85%.
×100%=85%.
(3)设5g盐酸中溶质的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 73
0.5g x
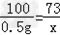
x=0.365g
稀盐酸的溶质的质量分数= ×100%=7.3%
×100%=7.3%
(4)设生石灰的质量为y,
CaCO3 CaO+CO2↑
CaO+CO2↑
100 56
50t×85% y
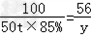
y=23.8g
答:生石灰的质量是23.8g
