问题
计算题
资料显示:碳还原氧化铁的过程如下:

如图所示的实验中,反应前氧化铁和碳粉的质量分别为32克和1.2克,反应后得到气体A和28.8克黑色固体B.
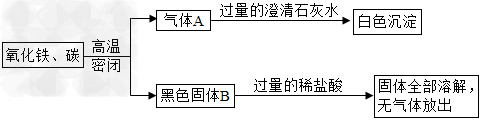
(1)求白色沉淀的质量;
(2)推断黑色固体B的化学式.(要求写出推断过程)
答案
解:(1)由题意可知,生成的气体A是二氧化碳,生成二氧化碳的质量=32g+1.2g﹣28.8g=4.4g
设生成白色沉淀的质量为x
CO2+Ca(OH)2=CaCO3↓+H2O
44 100
4.4g x
 ,
,
x=10g
(2)根据现象判断黑色固体没有铁和碳.
氧化铁中含铁元素的质量=32g× ×100%=22.4g;
×100%=22.4g;
根据反应前后元素种类不变,则B中铁元素的质量为22.4g,
则黑色固体B中含氧元素的质量=28.8克﹣22.4克=6.4g
若固体B的化学式为FexOy,由化合物中原子的个数比 ,
,
则x:y= :
: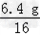 =1:1;
=1:1;
固体B的化学式为:FeO
