问题
计算题
将8g铁和铜的混合物加入到足量的稀硫酸中,充分反应后,只生成氢气0.2g.求:
(1)原混合物中铜的质量分数;
(2)反应后所得溶液中含铁的化合物的质量.
答案
设参与反应的铁的质量为x,生成的FeSO4质量为y,
Fe+H2SO4=FeSO4+H2↑
56 152 2
x y 0.2g
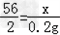 ,
,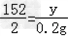
解之得:x=5.6g,y=15.2g,原混合物中铜的质量分数为: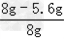 ×100%=30%;
×100%=30%;
答:(1)原混合物中铜的质量分数为30%;
(2)反应后所得溶液中含铁的化合物FeSO4的质量15.2g.
