问题
计算题
在某温度下,将36.5gCaCl2和NaCl的混合物放入230g水中使其完全溶解,再加入132.5g溶质质量分数为20%的Na2CO3溶液,恰好完全反应.试计算:
(1)生成的CaCO3沉淀多少克?
(2)反应后所得溶液溶质质量分数是多少?
答案
解:设生成的碳酸钙质量为x,生成氯化钠的质量为y,参加反应的氯化钙质量为z.
Na2CO3 +CaCl2 =CaCO3↓+2NaCl
106 111 100 117
26.5g z x y

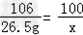
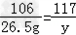
x=25g
y=29.25g
z=27.75g
反应后所得溶液溶质质量分数= %=10.2%
%=10.2%
答:(1)生成碳酸钙的质量为25g.
(2)反应后所得溶液溶质质量分数为10.2%.
