(8分).1994年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。臭氧能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图:呈V形,两个O—O键的夹角为116.5°。三个原子以一个O原子为中心,与另外两个O原子分别构成非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键(虚线内部)——三个O原子均等地享有这4个电子。请回答:
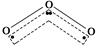
(1)题中非极性共价键是________键,特殊的化学键是________键。
(2)臭氧与氧气的关系是____________________。
(3)下列分子中与O3分子的结构最相似的是( )
A.H2O
B.CO2
C.SO2
D.BeCl2(4)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有______对孤对电子。
(5)O3具有强氧化性,它能把PbS氧化为PbSO4而O2不能,试配平:
________PbS+________O3===________PbSO4+_______O2,生成1 mol O2,转移电子的物质的量为________mol。
(1)σ 大π/π (2)同素异形体 (3)C (4)5 (5)1 4 1 4 2
(1)臭氧分子中非极性共价键都是单键,属于α键;特殊的化学键是大π键。
(2)氧气和臭氧都是氧元素形成的不同单质,所以互为同素异形体。
(3)氧元素和硫元素都属于第ⅥA,因此SO2的结构和臭氧最相似,答案选C。
(4)根据臭氧的结构可知。中间碳原子还有1对电子没有参与成键。两端的氧原子分别还有2对电子没有参与成键,所以共计是5对。
(5)PbS中S元素的化合价从-2价升高到+6价,失去8个电子;臭氧中只有1个氧原子得到电子,化合价从0价降低到-2价,所以根据电子的得失守恒可知,配平后的系数依次是1、4、1、4;根据方程式可知,生成1 mol O2,转移电子的物质的量为2mol。
