某课外活动小组的同学,研究用过量的锌与浓硫酸反应制取二氧化硫的有关问题:
(1)锌与浓硫酸反应制取二氧化硫的化学方程式为___________ _____ _________。
(2)这样制取的二氧化硫气体中可能含有的杂质是 ____________ ;原因是____ ________________________________ ___。
(3)某同学用下列装置连接成一整套实验装置以验证(2)的判断是否正确,若按气体从左到右流向时,气体流经的各装置导管的编号依次是 (用a、b……填写)。
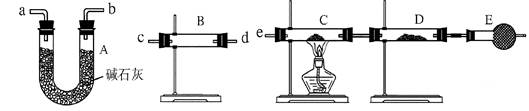
(4)根据(3)确定的实验过程,请将实验时有关装置中所盛药品、实验现象、结论或解释填入下表:
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | |||
| C | CuO固体 |
(共11分)(1)Zn+2H2SO4(浓)= ZnSO4+SO2↑+2H2O ( 2分)
(2)氢气和水蒸气( 1分) 随着反应的进行浓硫酸被消耗会变成稀硫酸,锌与稀硫酸反应产生氢气,同时会有少量水蒸气 ( 2分)
(3)c d (或d c) a b (或b a) e ( 1分)
(4) (各1分,共5分)
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | 无水硫酸铜 | 固体由白色变成蓝色 | SO2中含有水蒸气 |
| C | 固体由黑色变成红色 | SO2中含有氢气 |
(1)浓硫酸具有强氧化性,和锌反应的方程式是Zn+2H2SO4(浓)= ZnSO4+SO2↑+2H2O。
(2)生成的SO2中一定含有水蒸气。又因为在反应过程中,浓硫酸的浓度会逐渐变稀,所以还会生成氢气,即SO2中含有的杂质是氢气和水蒸气。
(3)水蒸气的检验用无水硫酸铜,氢气的检验用加热的氧化铜,因为氢气还原氧化铜生成水。所以在和氧化铜反应之前,需要首先检验水蒸气,且还需要除去水蒸气,所以正确的顺序是c d (或d c) a b (或b a) e。
(4)根据(3)中的分析可知,正确的答案应该是
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | 无水硫酸铜 | 固体由白色变成蓝色 | SO2中含有水蒸气 |
| C | 固体由黑色变成红色 | SO2中含有氢气 |
