I.根据下列化学方程式回答问题:
SiO2+2C+2Cl
SiCl4+2CO △ .
(1)12gC参与反应时电子转移的数目是______.(2)在该反应中,氧化剂是______.
II.请写出下列反应的化学方程式或离子方程式.
(1)在制作印刷电路板的过程中常利用铜与氯化铁溶液反应的离子方程式______.
(2)利用铝与二氧化锰反应来制取高熔点金属锰的化学方程式______.
III.某化学兴趣小组拟从海带中提取碘,进行如下实验:干海带
海带灰灼烧
浸泡液浸泡 过滤
I2(CCL4)→I2氧化 萃取分液
从A~C中选择适当的装置填空(填字母):
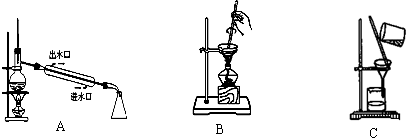
(1)过滤操作时用到的装置是______.
(2)从I2的CCl4溶液中提取单质I2并回收CCl4的可用装置______.
I.(1)12gC是1mol,碳由0价升高到+2价,故电子转移的数目是2NA;氧化剂是化合价降低的物质,Cl2的化合价降低,故答案为:2NA;Cl2 ;
II.(1)铜与氯化铁溶液反应生成2FeCl2和CuCl2,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)根据铝热法冶炼金属的原理:金属氧化物与铝反应得到金属和氧化铝,所以铝和MnO2反应的化学方程式为4Al+3MnO2
2Al2O3+3Mn, 高温 .
故答案为:4Al+3MnO2
2Al2O3+3Mn; 高温 .
III.(1)根据图形判断,C是过滤实验装置实验,故答案为:C;
(2)因CCl4易挥发,可用蒸馏的方法分离出CCl4,故答案为:A.
