加热氯酸钾和二氧化锰固体混合物制取氧气时,如果反应前氯酸钾和二氧化锰混合物的质量为3克,加热到不再产生气体为止,剩余固体的质量为2.04克.则:
(1)反应能制得氧气多少克?体积为多少升?(此状态下氧气的密度为1.43克/升)
(2)原混合物中氯酸钾的质量分数为多少?
解:(1)反应能制得氧气质量=3g﹣2.04g=0.96g 反应能制得氧气体积=0.96g÷1.43g/L=0.67L
答:反应能制得氧气质量为0.96g,反应能制得氧气体积为0.67L
(2)设原混合物中氯酸钾的质量为X.
2KClO3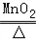 2KCl+3O2↑
2KCl+3O2↑
245 96
X 0.96g
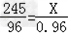
解得:X=2.45g
原混合物中氯酸钾的质量分数=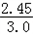 x100%=81.7%
x100%=81.7%
答:原混合物中氯酸钾的质量分数为81.7%
