为探究某抗酸药X的组成,进行如下实验:
查阅资料:
①抗酸药X可能的组成可以表示为:MgmAln(OH)p(CO3)q(SiO3)r(m、n、p、q、r为≥0的整数)。
②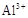 在pH=5.0时沉淀完全;
在pH=5.0时沉淀完全;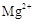 在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
实验过程:
| 步骤 | 实验操作 | 实验现象 |
| I | 向X的粉末中加入过量盐酸 | 产生气体A,得到无色溶液 |
| II | 向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,过滤 | 生成白色沉淀B |
| III | 向沉淀B中加过量NaOH溶液 | 沉淀全部溶解 |
| IV | 向II得到的滤液中滴加NaOH溶液,调节pH至12 | 生成白色沉淀C |
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是 。
(2)II中生成B反应的离子方程式是 。
(3)III中B溶解反应的离子方程式是 。
(4)沉淀C的化学式是 。
(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,则X的化学式是 。
(1)CO2
(2)Al3++3NH3·H2O ="=" Al(OH)3↓+3NH4+
(3)Al(OH)3+OH—="=" AlO2—+ 2H2O
(4)Mg(OH)2 (5)Mg3Al2(OH)10CO3
题目分析:(1)向X的粉末中加入过量盐酸产生气体A,得到无色溶液,说明含有CO32-、没有SiO32-。可能发生的反应为:CO32-+ 2H+== CO2 ↑ + H2O,SiO32-+2H+=H2SiO3↓。Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是CO2。向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,生成白色沉淀B,根据Al3+在pH=5.0时沉淀完全,Mg2+在pH=8.8时开始沉淀,pH=11.4时沉淀完全说明含有Al3+.生成B反应的离子方程式是Al3++3NH3·H2O ="=" Al(OH)3↓+3NH4+.向沉淀B中加过量NaOH溶液,沉淀全部溶解,这时发生反应Al(OH)3+OH—="=" AlO2—+ 2H2O。向II得到的滤液中滴加NaOH溶液,调节pH至12,生成白色沉淀C,说明含有Mg2+,Mg2++2NH3·H2O ="=" Mg(OH)2↓+2NH4+.沉淀C的化学式是Mg(OH)2。(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,n(CO2):n(Al(OH)3):n(Mg(OH)2)=1:2:3,则n(CO32-):n(Al3+):n(Mg2+)=1︰2︰3,假设n(CO32-)=1mol.再根据物质呈电中性可知还应该含有OH-离子,其物质的量为10mol。则X的化学式是Mg3Al2(OH)10CO3。
