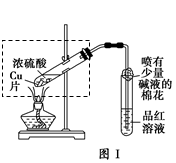
某校化学兴趣小组在探究铁与浓硫酸的反应时,将教材中铜与浓硫酸反应的实验装置(图Ⅰ)改为下图Ⅱ所示的装置。
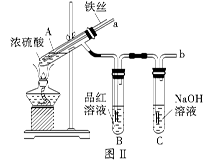
请回答下列问题:
(1)写出图Ⅰ中虚框处发生反应的化学方程式_________。
(2)图Ⅱ实验装置与图Ⅰ相比较,其优点是:①能更好地吸收有毒气体SO2,防止其污染环境;②_________。
(3)下列对导管a的作用分析中正确的是_________ (填字母)。
A.加热反应过程中,可上下移动导管a,起搅拌作用
B.停止加热,试管内的压强减小,从导管a进入的空气可增大试管A内的压强,防止倒吸
C.停止反应,撤装置之前往导管a中通入空气,可排除装置内的SO2气体,防止其污染环境
(4)反应一段时间后,将试管A取下,然后将试管A中溶液倒入另一盛有适量水的试管D中。该小组同学为确定溶液中所存在的金属离子,进行下列探究过程。
①提出假设:
假设Ⅰ:只含有Fe3+。假设Ⅱ:_________。假设Ⅲ:_________。
②实验设计:
分别取少量试管D中溶液,选用提供的试剂,设计简单的实验检验溶液中所存在的金属离子。请填写下表空白(可以不填满,也可以增加)。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液。
| 步骤 | 所选试剂 | 现象及结论 |
| 1 | ||
| 2 | ||
| 3 |
(共12分)
(1)Cu+2H2SO4(浓)  CuSO4+2H2O+SO2↑(2分);
CuSO4+2H2O+SO2↑(2分);
(2)能随开随停,便于控制反应的进行(2分);
(3)BC (2分)
(4) ①假设Ⅱ:只含有Fe2+ (1分)
假设Ⅲ:同时含有Fe2+和Fe3+ (1分)
②(各1分)
| 步骤 | 所选试剂 | 现象、结论 |
| 1 | KSCN溶液 | 若溶液变红,则含有Fe3+; 若不变红,则不含有Fe3+ |
| 2 | 稀H2SO4、KMnO4溶液 | 若KMnO4溶液褪色,则含有Fe2+;若不褪色,则不含有Fe2+ |
题目分析:
(2)铁丝可进可出,便于控制反应的进行。
(3)铁丝可进出,起到搅拌的作用,玻璃导管没有搅拌作用。A错,选BC。
(4) ①若硫酸过量,得Fe3+;铁过量,得Fe2+;若过量一部分,同时含有Fe2+和Fe3+。
②Fe3+和KSCN溶液反应,溶液变红;Fe2+遇KSCN溶液不变红,加KMnO4溶液后,变红。
