某校化学兴趣小组在学习了过氧化钠性质后,进一步研究其与SO2反应情况,查阅相关资料知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有同学认为:CO2、SO2虽然都是酸性氧化物,但SO2具有较强的还原性,CO2无还原性,反应原理应该不相同,并设计如下实验进行探究。
(1)[提出假设]向一定量的过氧化钠固体中通入足量的SO2,对反应后的固体产物成分及反应原理提出如下假设:
假设一:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设二:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设三:反应后固体中____________ _____,证明 。
(2)[定性研究]
为验证假设三是否成立,兴趣小组进行如下研究,请你完成下表中内容
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取反应后的固体放入试管中,…… |
(3)[定量研究]通过测量气体的体积判断发生的化学反应,实验装置如下:
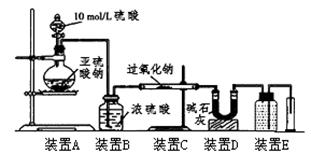
①装置D的作用是 。
②实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g,装置E中收集到的气体为VL(已换算成标准状况下),用上述有关测量数据进行判断
| SO2被氧化的程度 | V与m1或m2的关系 |
| 完全被氧化 | V=0 |
| 部分被氧化 | |
| 未被氧化 |
(1)固体为Na2SO3和Na2SO4的混合物,证明二氧化硫部分被氧化(每空2分,共4分)
(2)
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸。 | 加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解。 证明原固体中既有亚硫酸钠也有硫酸钠。 |
(3)①吸收未反应的SO2。(共2分)
②
| SO2被氧化的程度 | V与m1或m2的关系 |
| 完全被氧化 | V=0 |
| 部分被氧化 | 0<V<7m1/30 或m1>30V/7 |
| 未被氧化 | V=7m1/30或m1=30V/7 |
题目分析:(1)固体为Na2SO3和Na2SO4的混合物,证明二氧化硫部分被氧化;
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸。若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠。
(3)①D的作用吸收未反应的SO2。
②若Na2SO3未被氧化发生的反应只有2Na2O2+2SO2=2Na2SO3+O2根据差量法得到V=7m1/30或m1=30V/7,若部分被氧化发生的反应还有Na2O2+SO2=Na2SO4,该反应中SO2全部转化为固体的质量,没有气体生成,这个时候固体的质量增大,可知0<V<7m1/30 或m1>30V/7。
