已知Na2CO3的水溶液呈碱性.在一烧杯中盛有31.4g Na2CO3和NaCl组成的固体混合物,向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH______7(填>、=或<);
(2)通过计算求出烧杯中溶液恰好是中性时,所得溶液中溶质的质量分数.
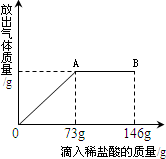
(1)根据质量关系图,滴入稀盐酸73g时,稀盐酸与溶液中碳酸钠全部反应生,溶液为氯化钠溶液呈中性,继续滴入稀盐酸则酸过量,中性溶液变成酸性;
故答:<;
(2)设固体混合物中碳酸钠的质量为x,生成氯化钠的质量为y,生成二氧化碳的质量为z.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x 73g×10% y z
106:73=x:7.3g,解之得x=10.6g
73:117=7.3g:y,解之得y=11.7g
73:44=7.3g:z,解之得z=4.4g
NaCl溶液中溶质的质量分数=
×100%=32.5%11.7g+31.4g-10.6g 31.4g+73g-4.4g
答:所得溶液中溶质的质量分数是32.5%.
