如图每一方框中的字母代表一种反应物或生成物。产物J是含金属元素A的白色胶状沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白。
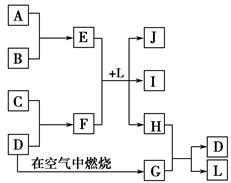
(1)框图中所列物质中属于非电解质的物质的化学式是 。
(2)用电子式表示出H的形成过程 。
(3)将E的水溶液蒸干并灼烧得到的固体物质的化学式为 。
(4)F的水溶液中各离子浓度由大到小的顺序为 。
(5)F的水溶液显碱性的原因: (用离子方程式表示)。
(6)E与F在L中反应的离子方程式为 。
(7)H和G之间反应的化学方程式为 。
(1)SO2
(2) 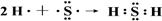
(3)Al2O3
(4)c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
(5)S2-+H2OHS-+OH-
(6)2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑
(7)2H2S+SO2=3S↓+2H2O
根据J是含金属元素A的白色胶状沉淀,可推断出A是Al,J是Al(OH)3;根据D是淡黄色固体单质,可推断出D为S。从图示转化关系知,E是含铝的化合物,F是含硫的化合物,结合I为NaCl溶液,可以推断出E是AlCl3、F是Na2S、L是H2O,则B 为Cl2,C为Na。G是SO2,结合SO2的性质及G与H的反应,可推断出H是H2S。(1)框图中只有SO2为非电解质。(3)AlCl3蒸干时水解得到Al(OH)3,灼烧最终得到Al2O3。(4)Na2S溶液中由于S2-水解溶液显碱性,离子浓度大小为c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)。(5)S2-水解的离子方程式为S2-+H2O HS-+OH-。(6)Al3+与S2-发生相互促进的水解反应:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑。(7)该反应为硫元素的归中反应:2H2S+SO2=3S↓+2H2O。
HS-+OH-。(6)Al3+与S2-发生相互促进的水解反应:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑。(7)该反应为硫元素的归中反应:2H2S+SO2=3S↓+2H2O。
