某研究小组欲探究SO2的化学性质,设计了如下实验方案。
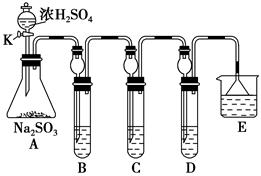
(1)在B中检验SO2的氧化性,则B中所盛试剂可为________。
(2)在C中装FeCl3溶液,检验SO2的还原性,则C中反应的离子方程式为_____________________________________________________。
(3)在D中装新制漂白粉浓溶液。通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分进行了探究。请回答下列问题:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1盐酸、0.5 mol·L-1H2SO4溶液、0.5 mol·L-1BaCl2溶液、品红溶液、新制澄清石灰水。
(ⅰ)假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为________;
假设三:该白色沉淀为上述两种物质的混合物。
(ⅱ)基于假设一,填写下表:
| 实验操作 | 预期现象和结论 |
| 将D中沉淀过滤,洗涤干净备用 | |
| 用另一干净试管取少量沉淀样品,加入______________ | _________________________ |
(ⅲ)若假设二成立,试写出生成该白色沉淀的化学方程式:
__________________________________________________。
(1)硫化氢水溶液(或硫化钠、硫氢化钠或相应溶质的化学式都可以)
(2)2Fe3++SO2+2H2O===2Fe2++SO42—+4H+
(3)(ⅰ)CaSO4
(ⅱ)
| 实验操作 | 预期现象和结论 |
| 过(适)量0.5 mol·L-1盐酸,塞上带导管的单孔塞,将导管另一端插入盛有少量澄清石灰水(或品红溶液)的试管中 | 若固体完全溶解,有气泡放出、且澄清石灰水变浑浊(或品红溶液褪色),则假设一成立。 若固体不溶解,或溶解但无气泡或澄清石灰水未变浑浊(或品红溶液不褪色),则假设一不成立 |
(ⅲ)2SO2+2H2O+Ca(ClO)2===CaSO4↓+2HCl+H2SO4
(1)~(2)涉及SO2的性质实验。SO2既有氧化性也有还原性,但多表现还原性(能够被氧化性稍强的Fe3+、H2O2或强氧化剂HClO等氧化),一般在和H2S等-2价硫化物反应时表现其氧化性,因此B中为H2S(或Na2S、NaHS等)溶液。
(3)探究白色沉淀的成分,其实是检验SO32—和SO42—。常通过与非氧化性酸反应产生SO2使品红溶液褪色来检验SO32—或HSO3—。
