问题
填空题
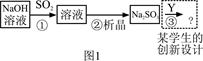
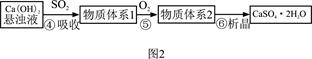
下图1是工业上“碱法烟气脱硫法” 示意图,下图2是工业上“石灰→石膏烟气脱硫法”示意图,回答:
已知:
| 试 剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
(1)图1中,反应①的离子方程式为 ,之一是 。
(2)图2中,反应⑤的目的是稳定固化硫元素形成高价态的化合物,氧气的作用是 。该法的优点之一是 。
(3)“碱法烟气脱硫法”中的产物Na2SO3的稳定性不好,易使硫元素重新转化为挥发性污染物,为避免之,设计了③的反应,写出其化学方程式为 。
答案
(1)SO2 +2OH- =SO32- +H2O 成本高(或Na2SO3 不稳定等合理答案)
(2)作氧化剂 成本低(或Ca2SO4·H2O稳定等合理答案)
(3)2 Na2SO3 + O2 =" 2" Na2SO4
题目分析:(1)二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,离子方程式为SO2 +2OH- =SO32- +H2O,该法的缺点有成本高、生成的亚硫酸钠不稳定等
(2)反应⑤的目的是稳定固化硫元素形成高价态的化合物,所以氧气的作用是做氧化剂;对比(1),可得该法的优点是:成本低、生成的Ca2SO4·H2O稳定
(3)Na2SO3的稳定性不好,易使硫元素重新转化为挥发性污染物,所以将其转化为硫酸钠,提高其稳定性,化学方程式为2 Na2SO3 + O2 =" 2" Na2SO4
