以下两道计算题,请你任意选做一题;若两题都做了,则以第一道题计分.
(1)过氧化氢溶液长期保存会自然分解,使得溶质的质量分数减小.亮亮从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一些测定溶质的质量分数.他们取出该溶液51克,加入适量的MnO2,生成氧气的质量与反应时间的关系如图所示:
①计算该溶液中溶质的质量分数;
②反应结束后,MnO2的质量分数与反应前相比______(填“变大”或“变小”)
(2)某生产钙片的企业,作了一个户外广告,如图所示.根据相关
| 名 称:高钙片 主要成分:碳酸钙 化 学 式: 含 钙 量:75% (某医药公司出品) |
①试通过计算说明,该广告中的含钙量是否合理?
②经实验测定,高钙片中含钙的质量分数为30%,请你在不改动广告中数据的情况下,如何改动广告用语更为合适?
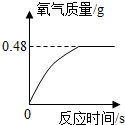
(1)①分析图象可知,放出氧气的最大质量是0.48克,设H2O2的质量是X.
2H2O2
2H2O+O2↑ MnO2 .
68 32
X 0.48g
═68 32 X 0.48g
得:X=1.02g.
溶质的质量分数为
×100%═2%1.02g 51g
②催化剂反应前后质量保持不变,随着氧气的放出,溶液的总质量变小,根据质量分数的计算公式(某种物质的质量分数=
×100%)可知,MnO2的质量分数与反应前相比变大,故答案为:变大.该物质的质量 各物质的质量和
(2)①碳酸钙中钙元素的质量分数=
×100%═40%<75%,因此广告不合理.40 100
②经实验测定,高钙片中含钙的质量分数为30%,这是合理的范围,高钙片中含钙的质量分数为30%,根据钙在碳酸钙的中含量可得碳酸钙在药品中的质量分数为
×100%═75%.所以要想不改动广告中的数据,可以把含钙量换成碳酸钙的含量.30% 40%
