问题
选择题
有一瓶无色气体可能含有CO2、HBr、NO2、HCl、SO2中的一种或几种。将此气体通入足量稀氯水中,恰好完全反应,得无色透明溶液,把此溶液分成两份,分别加入盐酸酸化了的BaCl2溶液和硝酸酸化了的AgNO3溶液,均出现白色沉淀,以下结论正确的是( )
A.不能确定原气体中是否含有SO2
B.原气体中肯定有HCl
C.原气体中肯定没有CO2
D.原气体中肯定没有HBr、NO2
答案
答案:D
无色气体中一定不含有NO2;气体与氯水反应后得无色透明溶液,气体中一定不含HBr;加入盐酸酸化了的BaCl2溶液和硝酸酸化了的AgNO3溶液,均出现白色沉淀,说明溶液中含有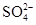 和Cl-,证明气体中一定含SO2,SO2+Cl2+2H2O=2HCl+H2SO4,则原气体中不一定含有HCl;没有现象证明CO2是否存在,A、B、C错误,D正确。
和Cl-,证明气体中一定含SO2,SO2+Cl2+2H2O=2HCl+H2SO4,则原气体中不一定含有HCl;没有现象证明CO2是否存在,A、B、C错误,D正确。
