问题
选择题
下列对有关实验事实的解释或得出的结论合理的是
| 选项 | 实验事实 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 | SO2具有漂白性 |
| B | 将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| C | 某钾盐溶于盐酸,产生无色无味气体,该气体通入澄清石灰水,有白色沉淀出现 | 该钾盐可能是K2CO3 |
| D | NaI溶液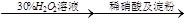 溶液变蓝色 溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
答案
答案:C
题目分析:A、KI淀粉溶液中滴入氯水变蓝,氯气氧化碘离子为碘单质,再通入SO2,溶液褪色,碘遇二氧化硫发生氧化还原反应而褪色,所以说明二氧化硫检验还原性,错误;B、将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3,是因为碳酸钠溶液为饱和溶液,硫酸钡的溶解平衡中部分钡离子与碳酸根离子结合生成碳酸钡就会沉淀析出,与Ksp(BaSO4)、Ksp(BaCO3)的大小无关,而且,若Ksp(BaSO4)>Ksp(BaCO3),则硫酸钡沉淀会全部转化为碳酸钡,错误;C、使澄清石灰水变浑浊的无色无味的气体是二氧化碳,所以该钾盐可能是K2CO3,正确;D、因为该过程中加的是硝酸,所以溶液变蓝色是否是H2O2的氧化性将碘离子氧化为单质碘还是硝酸的氧化性将碘离子氧化为单质碘,不能确定,错误,答案选C。
