近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(Ⅲ)将盐酸加入NaHSO3溶液中,反应所得到的SO2气体回收,生成的NaCl循环利用。
①写出步骤(Ⅰ)反应的化学方程式: 。
②写出步骤(Ⅱ)中电解饱和食盐水的化学方程式: 。
③写出步骤(Ⅲ)反应的离子方程式: 。
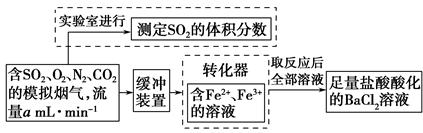
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42-的转化率。
①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是 。(填写序号)

A.碘的淀粉溶液
B.酸性高锰酸钾溶液
C.氢氧化钠溶液
D.氯化钡溶液②若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成SO 的转化率,已知气体流速,还需测定的数据有 、 。
的转化率,已知气体流速,还需测定的数据有 、 。
(1)①SO2+NaOH=NaHSO3
②2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
③HSO3-+H+=SO2↑+H2O
(2)①A、B ②实验时间 加入盐酸酸化的BaCl2溶液后生成沉淀的质量
求解SO2在混合气中的体积分数,需要求出两个量,一个是SO2的体积,一个是混合气的总体积。利用量气装置,可求出吸收SO2后余气的体积;利用洗气瓶中的X溶液,求出SO2的体积。所以对于洗气瓶中的溶液,必须能与SO2反应,且能发生明显的颜色变化,以便确定反应的终点。求解SO2的转化率,应求出SO2气体的总量和生成SO的量。因为在前一问中已求出SO2在混合气中的含量,所以只需确定混合气的总量。利用流速求总量,只需知道通入时间。要求SO2的转化率,只需确定沉淀质量。
