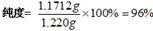芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸。反应原理:
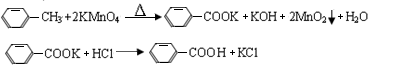
反应试剂、产物的物理常数:
| 名称 | 相对分子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | ∞ | ∞ |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |

图1回流搅拌装置 图2抽滤装置
实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在100℃时,反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
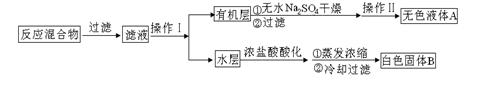
(1)仪器K的名称为 。无色液体A的结构简式为 。操作Ⅱ为 。
如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是 。
(3)下列关于仪器的组装或者使用正确的是 。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌棒下端不能与三颈烧瓶底、温度计等接触
C.抽滤结束后,为防止倒吸,应先关闭水龙头,再断开真空系统与过滤系统的连接
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入 ,分液,水层再加入 ,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220g产品,配成100ml溶液,取其中25.00ml溶液,进行滴定,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为 。
(1)安全瓶(1分)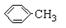 (2分) 蒸馏(2分)
(2分) 蒸馏(2分)
(2)除去未反应的高锰酸钾氧化剂,否则用盐酸酸化时会发生盐酸被高锰酸钾所氧化,产生氯气;(2分)
(3)ABD (2分)漏选得一分,错选不得分
(4) NaOH溶液(2分) 浓盐酸酸化(2分)
(5) 96% (2分
题目分析:
(1)仪器K为减压过滤(抽滤)装置中的安全瓶;
由实验流程可知,反应混合物首先经过过滤除去用高锰酸钾氧化甲苯后生成的MnO2
沉淀,过滤后的滤液经分液得到含有末反应的甲苯的有机层和含有苯甲酸钾等可溶性物质的水层。然后,将有机层经干燥剂干燥、过滤,再经蒸馏回收得到甲苯,所以无色液体A
为甲苯(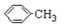 )。根据反应原理,可知水层中的
)。根据反应原理,可知水层中的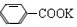 经浓盐酸酸化,转化为苯甲酸,因苯甲酸微溶于水,再经蒸发浓缩,冷却结晶,就可得到白色的苯甲酸晶体(无色固体B)。
经浓盐酸酸化,转化为苯甲酸,因苯甲酸微溶于水,再经蒸发浓缩,冷却结晶,就可得到白色的苯甲酸晶体(无色固体B)。
(2) 滤液呈紫色,说明滤液中含有末反应的高锰酸钾,亚硫酸氢钾是一种还原剂,先加亚
硫酸氢钾,是使其与高锰酸钾反应,除去末反应的高锰酸钾,否则当用浓盐酸酸化时,高
锰酸钾就会与浓盐酸反应产生氯气。
(3) 抽滤可以加快过滤速度,得到较干燥的沉淀;安装电动搅拌器时,搅拌棒下端不能与三颈烧瓶底、温度计等接触;抽滤结束后,为防止倒吸,应先断开真空系统与过滤系统的连接,再关闭水龙头;冷凝管中水的流向应是下进上出。C不正确,A、B、D正确。
(4) 甲苯不溶于水,要除去残留在苯甲酸中的甲苯时,先加入NaOH溶液,使其与苯甲酸反应,将苯甲酸转化为可溶性的苯甲酸钠,再经分液操作,将甲苯(有机层)除去,然后再用浓盐酸酸化,把可溶性的苯甲酸钠转化为苯甲酸。
(5) 根据反应: 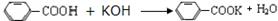
122g 1mol
m 2.4×10-3mol
m="122g/mol" ×2.4×10-3mol = 1.1712g;