问题
问答题
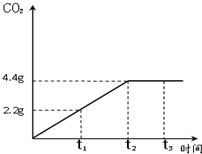
石灰石是百色老区丰富的矿产资源之一.某兴趣小组为测定本地石灰石中主要成份CaCO3的质量分数,称取12.5g的石灰石样品敲碎置于烧杯中,加入足量的稀盐酸,反应产生CO2的质量和时间关系如图(假设:石灰石中的杂质不与盐酸反应,也不溶于水 ).
请你仔细阅题和观察图象的数据,认真分析,解答下列问题:
(1)反应时间达到______时,碳酸钙与盐酸恰好完全反应;
(2)求石灰石样品中碳酸钙的质量分数.
答案
(1)由图象可知当反应进行到t2时生成的二氧化碳质量为最大值,此时即是碳酸钙和盐酸的恰好反应点;
(2)设12.5g样品中含有的碳酸钙质量是x
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
=100 x 44 4.4g
x=10g
则石灰石样品中碳酸钙的质量分数为
×100%=80%;10g 12.5g
故答案为(1)t2;(2)石灰石样品中碳酸钙的质量分数为80%;
