过氧化钠(化学式为Na2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O===4NaOH+O2↑。以下是某兴趣小组进行的探究活动。
(1)利用如下图所示实验装置制取氧气,请回答有关问题。
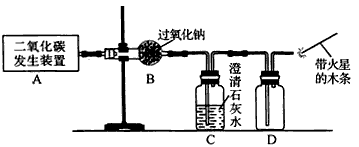
①实验室制取CO2的化学方程式为 。
②表明CO2未被Na2O2完全吸收的实验现象为 。
③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的哪些性质?
④若A装置产生的CO2中混有水蒸气,要检验干燥的CO2能否与Na2O2反应生成O2,以上实验装置应如何改进?
(2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验。
①有同学猜想X可能是酸、碱或盐中的一种。通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是 。
②同学们通过讨论和实验证明了X是Na2CO3。以下是他们设计的有关Na2CO3性质的探究实验,请根据卷首资料提供的信息,将下表填写完整。
| 实验操作 | 实验现象 | 有关的化学方程式 |
| 实验一:取少量固体样品, | ||
| 澄清石灰水变浑浊 | Na2CO3+2HCl===2NaCl+H2O+CO2↑ | |
| Ca(OH)2 +CO2===CaCO3↓+ H2O | ||
| 实验二:取少量固体样品,加水配成溶液, | ||
| 滴加适量的 溶液 | 有白色沉淀生成 |
(1)
①CaCO3+2HCl==CaCl2+H2O+CO2↑
②澄清石灰水变浑浊
③氧气密度比空气的大,氧气有助燃性。
④在A、B装置之间和B、C装置之间增加气体干燥装置(答出在A、B装置之间增加气体干燥装置即可)。
(2)①Na2O2和CO2都不含氢元素,根据质量守恒定律,二者反应后不可能生成含氢元素的酸或碱
② 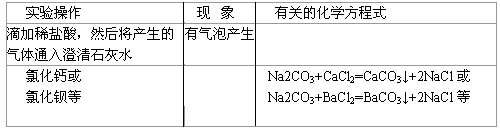
(3)解:设生成氧气的质量为x,生成氢氧化钠的质量为y。
2Na2O2+2H2O===4NaOH+O2↑
156 160 32
7.8g y x
X=1.6g Y=8g
氢氧化钠溶液中溶质的质量分数为: 8g/40g×100%=20%
