电子级钴的氧化物用于半导体工业和电子陶瓷等领域,是一种纯度很高的氧化物。其工业制取流程如下:
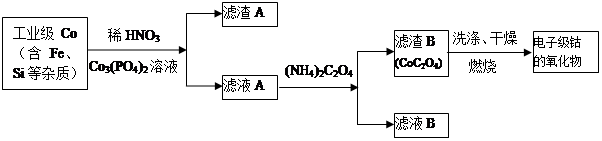
(1)实验室过滤所需的仪器有铁架台、铁圈、烧杯、 和漏斗。
(2)滤渣A的成分除过量的Co3(PO4)3和Fe(OH)3外还有 (填化学式),加入CO3(PO4)2的目的是 。
(3)Co与稀硝酸反应生成 Co2+的离子方程式为: 。
(4)滤渣B经过反复洗涤、干燥后,进行灼烧,其热重分析图如下:写出下列化学反应方程式:
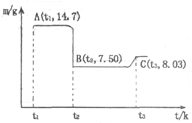
①AB段: ;
②BC段 。
(1)玻璃棒(2)Si 调节pH,保证Co2+不沉淀,而使铁离子全部沉淀
(3)3Co+8H++2NO3-=3Co2++4H2O+2NO↑
(4)CoC2O4 CoO+CO↑+CO2↑ 6CoO+O2
CoO+CO↑+CO2↑ 6CoO+O2 2Co3O4
2Co3O4
题目分析:(1)实验室过滤所需的仪器有铁架台、铁圈、烧杯、玻璃棒和漏斗。(2)在加入硝酸酸化时钴、Fe都与硝酸发生反应得到硝酸钴、硝酸铁而Si不能与稀硝酸发生反应,所以过滤后存在于滤渣A中。因此滤渣A的主要成分除过量的Co3(PO4)3和Fe(OH)3外还有Si。加入CO3(PO4)2的目的是调节pH,保证Co2+不沉淀,而使铁离子全部沉淀。(3)Co与稀硝酸反应生成 Co2+,根据质量守恒定律和电子守恒、电荷守恒,可知该反应的离子方程式为3Co+8H++2NO3-=3Co2++4H2O+2NO↑。(4)滤渣B(CoC2O4)灼烧发生分解反应:CoC2O4 =CoO+CO↑+CO2↑。得到固体为CoO。n(CoC2O4)=14.7g÷147g/mol=0.1mol;根据元素守恒可得m(CoO)=0.1mol×75g/mol=7.5g;而在t3时固体的质量为8.03g.根据质量守恒定律可知在BC段发生了反应:6CoO+O2
=CoO+CO↑+CO2↑。得到固体为CoO。n(CoC2O4)=14.7g÷147g/mol=0.1mol;根据元素守恒可得m(CoO)=0.1mol×75g/mol=7.5g;而在t3时固体的质量为8.03g.根据质量守恒定律可知在BC段发生了反应:6CoO+O2 2Co3O4。
2Co3O4。
