问题
填空题
有一无色透明溶液,欲确定是否含有下列离子: Fe2+、Mg2+、Al3+、Ba2+、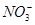 、
、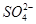 、Cl-、I-、
、Cl-、I-、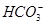 ,取该溶液进行实验:
,取该溶液进行实验:
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊试液 | 溶液变红 |
| (2)取少量该溶液加热,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定不存在的离子有 ,溶液中肯定存在的离子是 。
(2)请设计实验验证其中可能存在的阴离子的方法(写明操作、现象、结论) 。
答案
(1)Fe2+、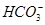 、I-、Ba2+;
、I-、Ba2+;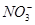 、
、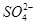 、Mg2+、Al3+
、Mg2+、Al3+
(2)Cl-的检验:取少量原溶液加足量的Ba(NO3)2溶液,过滤后,向滤液中加AgNO3溶液,生成白色沉淀,再加入稀硝酸,若沉淀不溶解可证明有Cl-
由步骤(1)的现象可知溶液呈酸性,故可以确定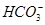 一定不存在。由步骤(2)的现象可知原溶液中一定含有
一定不存在。由步骤(2)的现象可知原溶液中一定含有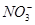 ,因
,因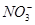 在酸性条件下具有强氧化性,故Fe2+、I-肯定不能存在。由步骤(3)知原溶液中一定含有
在酸性条件下具有强氧化性,故Fe2+、I-肯定不能存在。由步骤(3)知原溶液中一定含有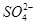 ,则Ba2+肯定不存在。由于步骤(3)中加入了BaCl2溶液,引入了Cl-,故步骤(4)中虽然产生了不溶于稀HNO3的白色沉淀,但不能说明原溶液中一定含有Cl-。由步骤(5)的现象可知原溶液中肯定有Mg2+和Al3+。由上述分析可知溶液中可能存在的阴离子为Cl-,检验时应首先用Ba(NO3)2溶液除去原溶液中的
,则Ba2+肯定不存在。由于步骤(3)中加入了BaCl2溶液,引入了Cl-,故步骤(4)中虽然产生了不溶于稀HNO3的白色沉淀,但不能说明原溶液中一定含有Cl-。由步骤(5)的现象可知原溶液中肯定有Mg2+和Al3+。由上述分析可知溶液中可能存在的阴离子为Cl-,检验时应首先用Ba(NO3)2溶液除去原溶液中的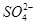 ,过滤后,向滤液中加入AgNO3溶液,再加入稀硝酸,若生成白色沉淀且不溶解可证明有Cl-。
,过滤后,向滤液中加入AgNO3溶液,再加入稀硝酸,若生成白色沉淀且不溶解可证明有Cl-。