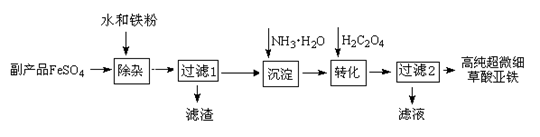
(16分)利用钛白工业的副产品FeSO4(含TiO2+、Al3+)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
(1)检验FeSO4是否已有部分氧化的方法是 。
(2)已知过滤1得到的滤渣的主要成分是Al(OH)3、H2TiO3。请补充化学方程式:
TiOSO4 + =H2SO4 + H2TiO3↓;铁粉的作用有:①除去溶液中的Fe3+,② 。
(3)沉淀反应的离子方程式是 。
(4)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 。FeC2O4生成后,为提高产品纯度,还需调节溶液pH=2,若pH过低,则导致FeC2O4的产率______(填“偏高”、“偏低”或“无影响”)。
(5)过滤2得到的滤液经蒸发浓缩、 、洗涤可得到副产品,该物质可用作 (写出一种用途)。
(16分,每空2分)(1)取少量副产品于试管中,加适量蒸馏水溶解,滴加1~2滴KSCN溶液,若溶液显红色,表明已有部分氧化。(若不全给1分)
(2)2H2O(能写出H2O 给1分) 与溶液中的H+反应,使Al3+水解完全生成Al(OH)3沉淀
(3)2NH3•H2O + Fe2+ =Fe(OH)2↓+2NH4+(配平错误或漏沉淀符号扣1分)
(4)NH3•H2O和Fe(OH)2受热都易分解;偏低 (5)冷却结晶、过滤;化肥
题目分析:(1)亚铁离子被氧化生成铁离子,可以通过检验铁离子验证是否被氧化,所以检验FeSO4是否已有部分氧化的方法是取少量副产品于试管中,加适量蒸馏水溶解,滴加1~2滴KSCN溶液,若溶液显红色,表明已有部分氧化。
(2)根据反应前后原子守恒可知,还缺少2分子水;由于溶液显酸性,而滤渣中含有氢氧化铝,因此要得到氢氧化铝必须降低溶液的酸性,所以铁的另一作用是与溶液中的H+反应,使Al3+水解完全生成Al(OH)3沉淀。
(3)滤液中的亚铁离子与氨水作用生成氢氧化亚铁沉淀,反应的离子方程式为2NH3•H2O + Fe2+ =Fe(OH)2↓+2NH4+。
(4)若温度过高则NH3•H2O和Fe(OH)2受热都易分解;若pH过低,则导致FeC2O4部分溶解,从而导致产率偏低;
(5)过滤2得到的滤液经蒸发浓缩、冷却结晶、洗涤可得到副产品硫酸铵,该物质可用作化肥。
