问题
实验题
甲苯氧化法制备苯甲酸的反应原理如下:
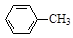 + 2KMnO4
+ 2KMnO4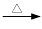
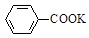 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
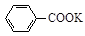 + HCl
+ HCl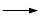
 +KCl
+KCl
实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100 ℃时, 反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。
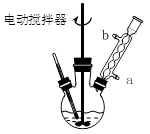
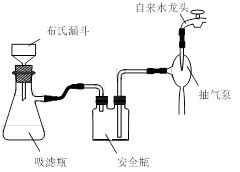
图1回流搅拌装置 图2抽滤装置
⑴实验室中实现操作Ⅰ所需的玻璃仪器有 、烧杯;操作Ⅱ的名称为 。
⑵如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是 。
⑶在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是 ;如图2所示抽滤完毕,应先断开 之间的橡皮管。
⑷纯度测定:称取1.220 g产品,配成100 mL溶液,取其中25.00 mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3 mol。产品中苯甲酸质量分数为 。
答案
⑴分液漏斗 蒸馏 ⑵过量的高锰酸钾氧化盐酸,产生氯气
⑶得到较大的苯甲酸晶粒,便于抽滤 抽气泵和安全瓶 ⑷96%(每空2分,共12分)
题目分析:⑴操作I为分液操作,其所需的玻璃仪器有分液漏斗、烧杯;操作II为蒸馏操作得无色液体A。
⑵为了避免过量的高锰酸钾氧化盐酸,产生有毒的氯气,应该先加亚硫酸氢钾除去过量的高锰酸钾,然后再加入浓盐酸酸化。
⑶为了得到较大的苯甲酸晶粒,便于抽滤,应该在抽滤前需快速冷却溶液;为了避免管道里的水在负压下回流,故在抽滤完毕,应先断开抽气泵和安全瓶。
⑷根据“1 ~1KOH”,则产品中苯甲酸质量分数为
~1KOH”,则产品中苯甲酸质量分数为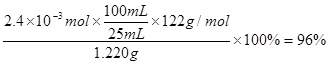 。
。
